(华东理工大学技术化学物理研究所)
1.引言
骨修复材料是指替补、修复人体硬组织的生物材料,广泛应用于骨外科、整形外科及牙科领域。骨缺损病人很多,仅我国每年就有数百万例。据美国高性能陶瓷市场的估计和预测,美国生物陶瓷的市场销售额1990年为1500万美元,每隔5年将以100%速度增长,2000年可达6000万美元。1996年世界生物陶瓷市场销售额将达到94亿美元。仅羟基磷灰石颗粒一项,日本莱昂公司1987年投放市场后,其早期销售额即接近2000万美元。因此,骨修复材料的研究和开发是全球关注的课题,是生物材料研究中一个非常活跃的领域。
经过二十多年来各国科学家的共同努力,已研制和开发出了多种骨修复材料,如氧化铝陶瓷、生物玻璃、磷酸三钙陶瓷、聚甲基丙烯酸甲酯(PMMA)骨水泥、羟基磷灰石(HAP)陶瓷等,其中PMMA由于其可塑性,在临床上用于肢体固定,HAP陶瓷由于其好的生物相容性已在临床上作为人造齿根、骨填充材料等。
但是研究开发和临床上应用的各种骨修复材料,包括自体骨移植、异体骨移植等,由于各自本身的缺陷而使其应用受到限制(如表1)。

自体骨移植是目前临床上用得最多的,效果好,但自体骨受来源数量限制、会引起二次手术痛苦、很难根据缺损部位准确塑型,并且植入后需要较长时间的爬行替代过程;异体骨存在不同程度的抗原性、会引起人体抗原抗体反应,同时也存在准确塑型难、须长时间爬行替代的问题;聚甲基丙烯酸甲酯(PMMA)骨水泥成型容易,但其固化过程是强放热的(高达110℃),会引起周围组织的坏死,生物相容性差,时间长后容易松动脱落;金属材料强度高,但与人体亲和性差;磷酸三钙陶瓷在人体内易被吸收造成缺陷。
人工合成的羟基磷灰石(HAP)与脊椎动物的骨和牙的矿物成分非常相近,且与人体组织有良好的生物相容性,故特别引人注目,近年发展非常迅速。羟基磷灰石陶瓷是将非生理pH值下形成的羟基磷灰石加热到800-1200℃制得的。这种加热过程能引起磷灰石晶体烧结,形成不被吸收的移植体。HAP陶瓷的应用受这种预成型材料的物理性质的限制;多孔HAP陶瓷(孔径200-500 pm)能使骨长入,但很易破裂,且很难使它的形状与需修复的缺损部位很好地吻合;HAP陶瓷颗粒很难仅仅局限在需要修复的部位,而且在组织长入之前,缺乏结构稳定性来维持所需要的形状。在实验上,已利用可吸收的连接材料如纤维牛胶原、纤维胶、硫酸钙等与HAP陶瓷颗粒结合来增强颗粒之间的接触,但这些混合物能提供的强度不够。总之对于HAP陶瓷,无论是颗粒型、多孔型还是块材,由于其成模难、烧结难和抛光难使得其在临床用中受到限制。
基于此,80年代中期布洛姆教授(E. Brom)及劳伦斯 · 邹(Lawrence Chow)在美国牙医学会设于美国国家标准和技术学院的研究室发明了自固化磷酸钙(Calcium phosphate Cement,简称CPC),它是由几种磷酸钙盐组成的混合物,能在人体的环境和温度下自行硬化,其成分最终转化为羟基磷灰石。目前美国、日本、西欧投入大量的人力物力对这种新型的生物材料进行了研究,但都停留在实验室阶段。
2.自固化磷酸钙的组成及特性
CPC是由固相和液相组成的复合体系,其中固相至少含除HAP以外的两种磷酸钙盐,磷酸钙盐包括磷酸四钙(TECP). α-磷酸三钙(α-TCP)或磷酸三钙(β_TCP)、二水磷酸氢钙(DCPD)、无水磷酸氢钙(DCPA)等。CPC的液相可以用蒸馏水、稀磷酸、生理盐水、手术部位的血液等。
CPC自行硬化并转化为HAP的原理,基于不同磷酸钙盐在水中的溶解度的差异,在pH4.2~11范围内,羟基磷灰石在水中溶解度最小,因而在热力学上是最稳定的。其他磷酸钙盐在水中会向HAP转化:
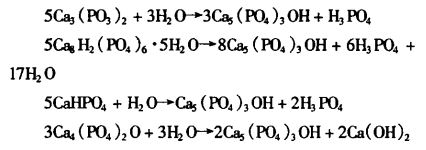
但是,这些单组分磷酸钙盐在水化时,有副产物酸或碱产生,使水化反应终止,因此单一磷酸钙盐的矿化能力是相当有限的。CPC是几种磷酸钙盐的混合物,它们之间颗粒大小和比表面积的合理匹配,可以保证反应始终维持在中性环境,避免pH羟基磷灰石陶瓷:偏移太大对组织损伤,并保持对HAP的稳定的过饱和度,提高了矿化能力。
总之,CPC是在人体的温度和水分条件下自行硬化并形成羟基磷灰石的。
与现有材料相比,CPC具有以下特点:
(1)生物相容性高,其成分最终转化为HAP,并且具有较高强度,因此继承了HAP陶瓷生物相容性好的优点,克服了PMMA的缺陷。
(2)操作方便,形状可以根据需要任意塑造,并可通过固化液的选择从而得到从5-30分钟完全硬化的时间域,固化后也可作外形修整。同时,固化时基本不放热,继承了PMMA可塑性优点,克服了其强放热损伤组织的缺损以及HAP陶瓷成型难、塑模难、抛光难的缺点。
(3)性能稳定,在人体环境中逐步被组织吸收并产生骨头再生效果,且生物降解速度同成骨速率相当,克服了自体骨、磷酸三钙陶瓷吸收降解过快、HAP陶瓷由于晶体烧结无法吸收、_V仅为高分子物质与人体骨不亲合、容易松动脱落、寿命不长等缺陷。
总之,好的生物相容性和能任意塑型的特性的有机结合使自固化磷酸钙克服了其他材料的缺陷,成为新一代的人体硬组织修复材料。
3.自固化磷酸钙的研究前沿
CPC是一种性能优异的人体硬组织修复材料,它的应用将使骨修复材料跃上一个新台阶,但其中有一些问题仍等待人们去探索。
首先,临床研究中发现有两点须进一步改进:(1)在骨瘤切除后的骨缺损治疗过程中,肿瘤细胞不一定清除干净,并有可能因肿瘤细胞局部转移查而导致治疗不彻底,旧病复发;2)若待植入部位感染,治疗效果差。基于此将抗癌或消炎等药物引入CPC中,利用药物定点缓释以提高治疗效果、简化用药方式、降低毒副作用,使材料在填充修复的同时也具有进一步治疗的目的。研究表明,通过CPC与药物的直接结合或与载药物微胶囊结合,可保持用药效果15天以上,材料性能跃上一个新的台阶,应用前景良好。
其次,抗压强度是自固化磷酸钙重要的性能指标,目前国外文献报导的最高值为65.3 Mpa,介于密度骨与松质骨之间,但在临床应用中仍显不足。借鉴陶瓷材料、水泥材料的增强机理,采取多种途径来提高CPC固化后的强度,以拓展CPC作为骨修复材料的应用领域和范围。我们在原有的基础上将CPC的抗压强度值又提高了一个水平:最高抗压强度可达96.5 Mpa比文献值高30 MPa;径向拉伸强度最高可达26.9 MPa,比文献值高近17 MPa。
第三,CTC作为良好的硬组织修复材料,填充性能优异,但其粘结性差,不能广泛用于骨折等常见硬组织损伤。如果利用自固化磷酸镁(MPC)体系高早强、粘结性强的特点,将其与CPC复合,开发出新一代骨粘结剂,将有望成为硬组织修复材料的里程碑。
4.自固化磷酸的产业化
由于生物材料最终以治疗为目的,它不可避免地与人体的组织、血液相接触,为了确保人身安全,防止材料植入体内及临床应用时引起不良生物反应,必须对材料的安全性进行较全面的评价,同时了解材料植入体内后功能的发挥情况。
对于材料的安全性评价,各国都制定了不同的标准,如美国的FDA标准,ISO94标准及我国1994年制定的医用材料评价标准等有一系列的评价指标。
通过对材料的安全性考察发现CPC无毒、无致癌、致突变、致畸形,与有机体亲和性好。同时,将其用于新西兰大白兔股骨非负重部位的填充修复并进行了组织学评价。CPC植入体内后血钙、血磷和碱性磷酸均处于正常水平,没有引起代谢紊乱。植入两周后材料表面轮廓分明,界面清晰,并有一定强度的连接。植入1个月后材料与骨已形成紧密连接,两端被骨膜成骨覆盖,无炎症反应或纤维膜形成。植入3个月后已有部分新生骨长入,6个月后植入材料同宿主骨相邻边缘被新生骨取代。12个月以后,从CPC骨界面上可见CPC的降解伴随着新骨长入,同时发现CPC内部也发生降解,降解的CPC孔内形成孤立的骨岛。整个过程表明CPC在骨膜下能诱导新骨生成,材料具有可降解性,是一种生物相容性好、性能优异的骨修复材料。上海医科大学附属中山医院等单位对一期临床病例的追踪调查显示,材料植入后无毒、无刺激,能满意地修复骨缺损。
高的生物相容性和能根据缺损部位任意塑型并自行硬化的特性的结合,使自固化磷酸钙成为优异的骨修复材料,可广泛应用于骨科、脑外科、牙科、整形外科等领域。目前,集产品的研制、开发、生产和营销为一体的上海瑞邦生物材料有限公司已宣告成立,瑞邦公司致力于自固化磷酸钙等产品的推广作用,更好地为临床服务,造福社会。