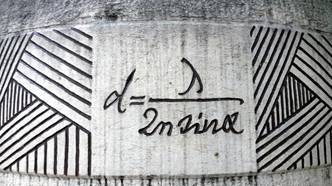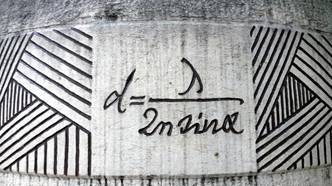功能强大的超分辨率显微镜允许研究者在纳米尺度下探索世界,势必改变我们对于细胞的认识。
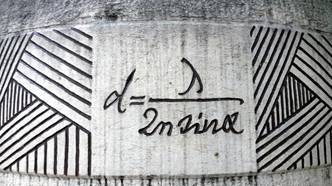
在德国耶拿,光学物理学家恩斯特·阿贝的纪念碑上镌刻了描述衍射极限的方程式
戴奇·马林斯(Dyche Mullins)戴上了一副Oculus公司生产的Rift 3D虚拟现实眼镜,顿时从加州大学旧金山分校的一个格子间进入了虚拟世界。透过这套虚拟现实眼镜,马林斯见到了一个看起来仿佛有儿童般大小的免疫细胞。这个细胞缓缓穿过一片骨胶原纤维构成的迷宫。马林斯可以移动画面,推进镜头(这样中性粒细胞仿佛直接在他上方蠕动),或者转动画面,从不同角度观看细胞的移动。
这并非仿真模拟。这段视频是用一种前沿的显微镜摄制的,它的发明者叫埃里克·白兹格(Eric Betzig),是弗吉尼亚州阿什本霍华德·休斯医学研究所下属珍利亚研究园区的一名工程师。细胞迁移方面的基础性工作始于上世纪50年代和60年代在二维、低分辨率和载玻片条件下的研究。马林斯是名分子生物学家,他表示更清晰地看见细胞有助于推翻那些早已被普遍接受的基础知识,譬如细胞如何迁移,它们到底是在组织中移动的免疫细胞,还是在池塘中移动的阿米巴虫。有了最新的成像工具,他就能观看到细胞移动时生动的细节。
这些工具重新定义了显微镜学的研究前沿,它们对生物学的潜在影响力难以估量。超分辨率显微镜的研发始于2000年,在那之前,生命最基础的分子世界在人类眼中一团模糊,仅能用相对低分辨率的光学显微镜略作观察,或者用清晰但却只能获得静态单幅图像的电子显微镜。“现在我们有证据表明这些障碍是可以克服的。我们刚刚在起点上,有可能做成一些事。”斯特凡·黑尔(Stefan Hell)说道,他是德国哥廷根马克斯·普朗克生物物理化学研究所的一名主管。黑尔是一位新晋的诺贝尔奖得主,在今年第65届林道诺贝尔奖得主会议上,他发表了这个主题的演讲,让参加会议的其他诺贝尔奖得主及年轻科学家们激动不已。
因为研制出超分辨率荧光显微镜,黑尔与埃里克·白兹格、威廉·莫纳尔(William Moerner)一起获得了2014年诺贝尔化学奖。在他们的研究工作之前,生命移动时的纳米尺度细节从未被人类目睹过。那儿是一大片盲区。生命是动态的:细胞不仅会像马林斯观察的中性粒细胞那样到处爬来爬去,还会分裂,会从一个细胞的内部结构(或者说细胞器官)运送化合物到另一个细胞里,诸如此类的行为还有很多。除了细胞迁移,研究者还会利用超分辨率显微镜观察一群病毒攻击一个细胞时的实时场面,他们将这些仪器对准大脑神经元之间的化学连结。“这项技术会让一切改观。我准备好把我的其他仪器放到eBay上卖掉了。”托马斯·基尔希豪森(Tomas Kirchhausen)说道,他是麻省波士顿哈佛医学院的一名细胞生物学家,也是这些工具的另一名早期使用者。

因为超分辨率显微镜方面的工作,斯特凡·黑尔与另两名科学家一起被授予了诺贝尔奖
更锐利的图像
黑尔是打破光学显微镜实际存在极限第一人。然而,他告诉林道诺贝尔奖得主会议上的听众,在不久之前,还没人把他的看法当回事(诺贝尔奖得主常说这种话)。成像极限的观念不仅深植在科学家的头脑里,实际上还铭刻在石头上。黑尔在讲座的屏幕上出示了一张照片,照片里是一位科学前辈恩斯特·阿贝的纪念碑,位于德国耶拿――这块纪念碑上镌刻了描述衍射极限的方程式。
阿贝出身卑微,最终成为德国显微镜制造商蔡司公司一位杰出的光学物理学家。黑尔解释说,阿贝是第一个弄明白光学显微镜成像原理的人,他能够制造出最精良的显微镜。阿贝琢磨出当一束光线聚焦在一个尺寸比光的波长一半更小的点上,光开始与其自身干涉,图像也随之变得模糊。如果两个物体之间的距离小于那段距离――200纳米――常规的光学显微镜无法分辨这两个物体,无论镜片有多完美。这就是阿贝的衍射极限。
光学显微镜能成为强大的研究工具,很大程度上要感谢阿贝做出的贡献。“我对阿贝满怀敬意。”黑尔说道,他把自己建在德国哥廷根的显微镜公司命名为“阿贝维尔”。阿贝并没弄错,那是所处时代的产物。1873年,阿贝发表了他在衍射极限方面的研究,当时分子是尚未得到证明的想法,制造更好的显微镜完全取决于光学上的进展。
黑尔意识到化学能让研究进一步深入。在衍射极限之下,是丰富多彩的微生物世界,包括了病毒、蛋白质和细胞器官(譬如生成能量的线粒体)的细节。黑尔执迷于突破衍射极限并决定揭露出这个世界。他的研究重心放在一项名叫荧光显微学的技术上,生物学家常常运用这项工具。它是光学显微镜学的一种形式,通过荧光化学标签来增强功能。这些明亮的红色、绿色或其他颜色的标签附着在生物学家感兴趣的特定分子上,起到标记的作用,帮助确定特定类型细胞或细胞内结构的位置。
在上世纪90年代,黑尔读到一篇介绍“受激发射”的量子力学现象的文章――一种控制这些标签的荧光的方法――仿佛被电击了一般。他意识到,成像不仅仅在于精良的镜片,也可以使用化学手段来越过衍射极限。
黑尔设计出一套使用到两束光线的系统,一束光线激发荧光分子,另一束光线立刻关闭大多数荧光分子,使得仅有那些处于光束中心的荧光分子继续发光。他把这项技术称为“受激发射损耗(STED)”显微技术,按照黑尔的说法,它并未打破衍射极限,而是玩了套把戏,绕过了衍射极限。结果形成了圆筒状的光束,外形就像甜甜圈的轮廓,只不过内圈也被光填满。接着,用这种光束扫描样本,获得完整的图像。黑尔在2000年制造出的第一台超分辨率显微镜仅仅超过衍射极限大约两倍,但它终究突破了障碍。
黑尔形容自己是一名梦想者,在他做出这一荣获诺贝尔奖的发现之前,他感觉自己隔离在科学界主流之外。然而,白兹格有着一名古怪局外人的气场,在今年林道会议上发表的演讲中,他清楚地表明自己对学术界的束缚没有耐性。白兹格称自己是一名“工具建造者”――一位想要建造出最好的显微镜的工程师。
长久以来,白兹格也痴迷于超越阿贝衍射极限这件事。上世纪90年代初,他在新泽西莫雷山著名科研中心贝尔实验室里做近场显微镜研究,并在一项名叫近场成像的技术上取得了进展。但他认为这不是一种非常有用的工具,却还要对其做研究,从而感到越来越气馁。近场显微镜在技术上击败了衍射极限,但它并不是非常实用,因为它用到一根尖锐的成像探针,必须与样本离得非常近才行。白兹格一度离开科研有数年之久,在父亲的公司里工作,设计机械加工装备。在创造出一个公司卖不出去的设计方案后,他遭遇了所谓的第二次中年危机。白兹格一直紧跟科技文献,当读到绿色荧光蛋白质的资料后,他回到了科学界,回到了莫纳尔正在引发争议的同一块领域,也就回到了衍射极限这个难题上。
像黑尔的解决办法一样,白兹格的方法也依赖化学,具体说来就是莫纳尔正在研究的一种名叫光切换的现象。莫纳尔在加州圣何塞IBM工作,是第一个测量单个分子吸收光谱的人。1997年,他的研究进一步表明,某些荧光分子可以用光束开启或关闭。支撑这种发现的物理学与STED技术不同,但含义是相同的:研究者能够开启或关闭荧光分子,就好像它们是电灯泡一样。
黑尔的显微镜用一种狭窄的光束来扫描样本,逐一填满图像区域,然而白兹格的研究工作结合整个成像区域的多张模糊的快照,来拼凑出完整的图片。在白兹格使用的方法中,每次图像捕捉之前,显微镜用一种微弱的光束照射样本,它只会开启样本中一小部分的荧光分子。这种步骤不断重复,直到所有分子的位置都已确定为止。就算两个分子之间的距离低于衍射极限,它们也会出现在不同的子图像中,这样两个分子在最终的合成图像中都能看到。
焦点上的细胞
试用新技术的生物学家们会惊叹如今的技术所能实现的奇迹。在17世纪,罗伯特·胡克把一片软木放到他制作的显微镜下仔细观察之前,他并不知道细胞的存在――当时世上没人知道细胞的存在。但细胞确实存在。“……这是我见到过的第一个微观毛孔,或许是世人见到过的第一个,因为我尚未见过哪本书或哪个人在此之前提及过这些微观毛孔。”胡克在1665年如此写道。超分辨率成像技术早期使用者们的故事让人联想起胡克。“超分辨率不仅仅是获得更锐利的图像。你可以发现以前从未见到过的东西。”庄小威说道,她是哈佛大学的一名生物物理学家,发展了另一种名叫随机光学重构显微法(STORM)的超分辨率方法,她和同事在2006年发表了这一成果。

庄小威发明了一种超分辨率显微镜方法STORM
庄小威在2012年运用STORM观察神经元中的结构性肌动蛋白,见到了一些让人惊异和耳目一新的现象。庄小威对突触有着研究兴趣,突触是神经元之间的电化学连结,是脑电路中的基本单位。她让自己手下的博士后研究员生成突触结构的图像,以高分辨率标示出肌动蛋白。但图像最显眼的特点在于突触旁边:图像里的轴突(传递神经元向外发出的信号的修长突起)看起来很古怪。
研究团队沿着轴突看见了规则排列的肌动蛋白环。“这是一种让人瞩目的周期性结构――每180纳米就会出现一个肌动蛋白环。”庄小威说道,“布置得很美丽,看起来简直就像水晶的结构。”这种式样的特征尺寸小于衍射极限,所以肌动蛋白环以前一直是不可见的。在常规的荧光显微镜下,你可以看见一块斑点,表明肌动蛋白的存在,但周期性排列的环状结构一团模糊,而在庄小威的STORM显微镜下就清楚可见。也没有人在电子显微镜下注意到这些环状结构,因为细胞里的其他纤维结构掩藏了环状结构。
庄小威发现,肌动蛋白环在所有轴突上都存在,但仅在一小部分树突上呈现片状存在,树突是接收信号的神经突起。“轴突骨架”帮助轴突维持力学稳定,传导神经冲动。这种理解有其他研究的支持,研究表明,那些接受过基因改造、缺乏连结肌动蛋白环的蛋白质的蠕虫有着脆弱的轴突,移动功能受损,对力学刺激较无反应。
哈佛医学院的基尔希豪森使用白兹格制造的一台显微镜时,也有类似大开眼界的时刻。这台显微镜每次使用薄片状的光束来照射样本的切片,再采用白兹格的超分辨率方法来成像。这是白兹格的研究工作最近的一个实例。基尔希豪森已经花费了数十年来钻研一种被称为囊泡、直径仅有30~80纳米的薄膜泡的构成。囊泡携带化合物到细胞各个地方,也帮助细胞吞噬、输送和分解不想要的分子和微生物。2004年,基尔希豪森完成了第一幅蛋白质复合体结构从细胞膜上掐断囊泡的图像。他采用近原子级分辨率,用电子显微镜生成图像,最小距离压低到0.8纳米。但是,尽管他在判定囊泡结构方面取得了进步,他还是说:“我意识到我应该关注动态的东西。”他使用白兹格制造的一台显微镜,最终得以观看到整个过程。在30到90秒的时间里,数百个分子组装成一种弦线穹顶状物体,再脱离出一只薄膜泡。接着它们脱离开来,离开囊泡。基尔希豪森现在能观看这种在一个细胞内一分钟发生数千次的过程。
2014年,超分辨率显微镜刚刚上马运行,基尔希豪森就开始把它用于其他各种需要有三维超分辨率图像的研究项目。“我们把病毒随意撒到细胞上,再观察病毒如何进入细胞中。”他说道,“现在我们能追踪每个病毒,看它如何进入细胞,跟踪它的命运。”哪些病毒取得成功?哪些病毒失败了?病毒进入细胞时发生了什么事?这些是基尔希豪森如今可以提出的问题。
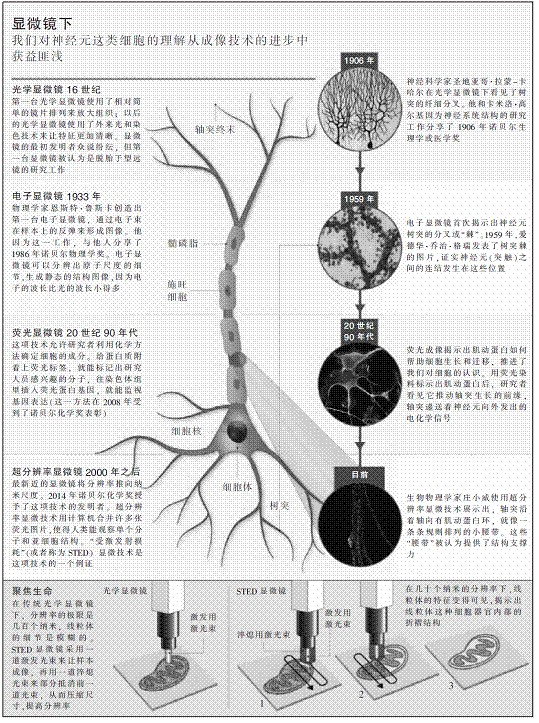
挑战还在前方
使用超分辨率显微镜并不像使用老式的光学显微镜。基尔希豪森说:“没有双筒目镜,一切都是在电脑上完成的。”马林斯说:“你可以看见从显微镜直接获得的原始版图像,但随后要花费一些时间,才能把那些图像表现成有用的结果。”这些方法的基础是一次让庞大数目的单个分子成像。若不是经过强大软件的预先处理,人类的眼睛或者大脑理解不了这些结果。
马林斯解释说,大多数图片处理软件都是设计用来处理二维、低分辨率图片的。他为了研究工作,与加州大学的三维图片处理方面的专家合作。中性粒细胞爬过两微米长的组织的视频是在一次为时三分钟的实验中获得的,却产生了25GB的数据。一部典型的好莱坞高清电影的大小约为它的十分之一。因此,数据分享和储存正在成为一个难题。
硬件是超分辨率显微镜使用上的另一项障碍。莫纳尔在他的实验室里使用的超分辨率显微镜基于白兹格和黑尔的设计方案,整个装置很复杂。一平方米左右的面积内,大约有30个精确放置的光学组件引导出成像光。显微镜必须放置在一张隔绝振动的桌子上,这种桌子在物理系很常见,但在湿式实验室里并不常见。
装置的这种脆弱性并不理想。包括蔡司公司和黑尔的创业公司在内的企业正在设计商业化的型号,将这些装置的更加紧凑、定型的版本装进一个箱子里。白兹格说,到目前为止,市场上的型号都不是非常让人满意,但情况会发生变化。
这种商业化的动向并不代表基础研究在放慢速度。黑尔说,他如今的梦想是以一纳米的分辨率实时标示出活体组织内的每一个蛋白质,而不会对组织引起任何损伤。庄小威的梦想与之相似。她的实验室的一项目标是在染色体组尺度下,追踪单个细胞内基因表达的变化――那会意味着在同一时刻让细胞内的所有信使RNA得以成像。2015年4月,庄小威发表了她初次尝试的成果,结合了单分子成像和计算学方法,同时侦测了一个细胞中大约1 000种不同类型的RNA分子。因为她的研究兴趣是大脑,她特别想看到神经元发育的过程,弄明白基因表达模式如何导致神经元的不同行为。
庄小威的另一个目标是追踪神经元在突触位置的通信,看到这些细胞与细胞之间的化学通信,同时电生理学家们能够测量单个神经元的电信号。她的一个研究项目是追踪单个神经元内的计算过程。目前,没人完全明白神经元如何整合输入信号,再生成输出信号。一旦这个问题获得单个细胞层面的解答,观测可以转向弄明白小型神经元电路里的计算过程,并最终弄清整个大脑里的计算过程。
目前,用这些方法让那些单个细胞成像是可以办到的,但要在组织层面获取快速、单分子分辨率的视频难度更大,譬如说大脑内的组织。当前的装置受到的阻力在于现有成像染料的亮度与开关响应,一次可以使用的色彩种类是有限的。

诺贝尔奖得主埃里克·白兹格研制出的显微镜捕捉到的一幅活细胞画面
为了帮助推进研究领域,庄小威、黑尔和其他成像研究者把目光投向了化学。“下一个研究前沿会是新染料颜色。”卢克·拉维斯(Luke Lavis)说道,他是珍利亚研究园区的一名化学家,开发了荧光成像标签。创造出能附着在生物分子上、又尽可能少地干扰它们的功能、并且制造出色彩如彩虹颜色那么丰富的染料,色彩要各自不同,能够在图像处理时予以区分,这样会让研究人员可以在同一时间看见更多移动中的分子。
并且,让染料更为明亮,或者精心地设计染料(让它们附着到目标上之后才发出荧光),这些手段可能会让细胞不再因为反复照射的高能激发光线而受到严重损伤。拉维斯正在对此进行研究。“我的研究刚起步时,研究人员会使用1888年就被人提出的合成法,但化学从那时起已经有了那么多发展。现在,我们真的能探索那些染料的结构。”他说道。
看着马林斯在3D眼镜里探索亚细胞世界,有一点是清楚的:今时今日的显微镜所展露的细节会让阿贝和胡克等研究先驱瞠目结舌。然而,超分辨率成像并不只是关于将细胞看成分子的集合体,并对其量化。“看到这一幕之前,我一点也不明白细胞的心理。”马林斯半开玩笑地说道。在视频里,细胞不是个抽象的物体。它会对力做出反应,也会施以回力。细胞成为了明显可见的物理存在。相比于以前查看细胞的所有方法,这种方式让细胞看起来更加鲜活。
资料来源 Nature
责任编辑 彦 隐