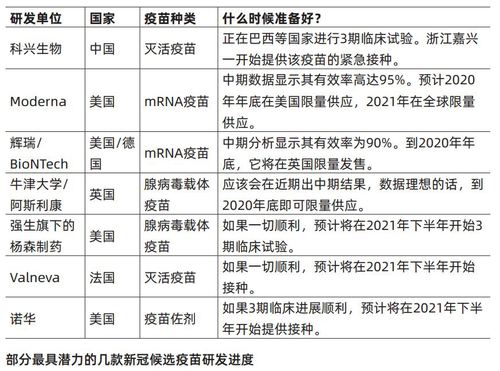
各团队的新冠疫苗研发工作热火朝天,且越来越逼近终点
2020年11月17日,《柳叶刀-传染病》(The Lancet Infectious Diseases)发表北京科兴中维生物技术有限公司(简称科兴生物)研制的新冠候选疫苗“克尔来福”(CoronaVac)的1/2期临床试验结果论文。临床数据显示,疫苗可触发快速免疫反应,在2期试验中,克尔来福两剂接种28天后,中和抗体阳转率达90%以上。换言之,中国团队的疫苗在这项700人参与的中期试验中显示出巨大成功。如论文作者之一、江苏省疾病预防控制中心副主任朱凤才所说,已有结果表明疫苗“适合紧急使用”。
虽尚未如Moderna和辉瑞/BioNTech那般发布大规模临床的中期数据,但目前克尔来福的研究团队正在巴西和东南亚开展3期临床试验,相信人们很快就能看到最终结果,而且用部分媒体人的话说,“没发布数据也并不意味着进度比别人慢”。值得一提的是,近期巴西曾因志愿者死亡而暂停克尔来福疫苗的试验,但在发现接种者死于自杀而与疫苗无关后,又恢复了试验。另一方面,土耳其等国家即将(或已经)与科兴生物签署新冠疫苗订购合同。
除了克尔来福,还有其他3款中国研发的新冠疫苗也都进入了3期临床试验,包括由中国医药集团中国生物技术股份有限公司(简称中生公司)开发的2支灭活疫苗,以及由军事科学院军事医学研究院和康希诺生物股份公司联合研制的腺病毒载体疫苗。前者开赴中东,接种超过3.5万志愿者,后者则获批在欧亚地区开展3期临床。
这几款疫苗都被申请或已经投入紧急使用,例如科兴生物约有90%的员工及家属已按中国的紧急使用方案接种克尔来福,康希诺正与多国接洽紧急使用批准,中生公司的疫苗则被阿联酋等国家特批给一线医务人员接种。
英国BBC的科学报道团队迅速跟进了克尔来福的进展,并表达了自己的观点:“通常,药物的1期和2期试验结果不会在实验室外引起人们的过多关注。这些阶段主要是为了检查该药物是否安全,以及是否有望在3期临床中奏效。科兴生物的疫苗与辉瑞/ BionTech和Moderna团队的疫苗不同,它由化学灭活的病毒制成,这是更为传统的开发方式。制造方强调了这样一个事实,即他们的疫苗在试验中产生了快速反应——志愿者在接种后的14天内即产生病毒抗体。研发团队认为,这种迅速的特点令其适合疫情暴发时紧急使用或适合医护人员使用。不过在得出关于其有效性的肯定结论前,我们应该等待目前在巴西、印度尼西亚以及土耳其进行的大规模试验的结果(预计12月完成中期分析)。当然,即便是要在不久后出来的,或是Moderna们已经发布了的第三阶段数据,还是需要被谨慎对待——在全面普及之前,没人知道它们当中的哪一个将长期有效。”
资料来源 BBC