此类基因疗法的简便性和高效率使其极具潜力,有望治疗像帕金森病这样的神经系统疾病。
近期,来自加州大学圣地亚哥分校的付向东团队在《自然》(Nature)发表文章表示,通过消解特定蛋白质,可使星形胶质细胞向神经元细胞转变,从而逆转帕金森病小鼠的病例症状。而在更早些时候,来自中国科学院杨辉团队也以相似的思路完成了神经元转变,并将研究成果发表于《细胞》(Cell)。毫无疑问,这两大重磅研究为人类攻克帕金森病开辟了全新的道路。
帕金森病模型小鼠的实验
皮肤细胞和星形胶质细胞可以通过强制表达(或过表达)转录因子、microRNA或小分子等方法在体外转化为其他类型的细胞,能诱导产生多巴胺的神经元(iDA神经元)便是其中一种细胞类型。目前已有科学家使用这种方法成功将小鼠大脑纹状体中的星形胶质细胞转化为了iDA神经元:这些小鼠身患帕金森病,同人类患者一样,中脑黑质里的iDA神经元都已变性死亡(该病最主要的病理特征);但经过实验,它们失而复得,小鼠的运动缺陷也因此得到了改善。
不过靠此方法得来的iDA神经元既无法形成健康大脑里应有的远距离神经元联结,也难以使患病小鼠的运动行为完全恢复正常。付向东团队选择了另一种策略,有效地将星形胶质细胞重编程为神经元,帕金森病小鼠的病情恢复也相对更为彻底。
该研究团队一开始对分离自小鼠大脑皮层和中脑以及人类皮质中的星形胶质细胞进行了体外实验。他们的目标是除掉星形胶质细胞里的PTB蛋白,以此促进星形胶质细胞转变为iDA神经元——PTB是一种具有剪接作用的多聚嘧啶序列结合蛋白,存在于星形胶质细胞当中,它的表达会抑制神经元分化。付向东等人此前已证实PTB蛋白越少,细胞越容易变成神经元。
他们采用的方法是破坏编码PTB蛋白的Ptbp1基因的转录过程。具体操作就是使用一种小发夹结构RNA(shRNA)降解掉那段能指导PTB蛋白合成的信使RNA。如此一来,数量多、易增殖,且具有高度可塑性的星形胶质细胞便可以最大限度地向iDA神经元转化,结果也确实如他们所愿。
值得一提的是,杨辉团队借助基因组编辑技术CRISPR–CasRx切掉了小鼠星形胶质细胞中Ptbp1基因的mRNA,也达到了相同的目标。(用具备CRISPR–CasRx能力的病毒感染小鼠的星形胶质细胞。)
体外成功之后就是体内实验。付向东团队使实验小鼠大脑中的星形胶质细胞可以被专吃Ptbp1基因的shRNA病毒靶向。shRNA病毒一来,PTB蛋白自然就销声匿迹了。最后的实验结果为:小鼠注射病毒后,20%的星形胶质细胞很快就转变为神经元;10周后,这个数字升高至80%;最喜人的是注射12周后,30%~35%的星形胶质细胞成为多种类型的iDA神经元。
iDA转化依托于多种转录因子
通过除掉PTB的方式让星形胶质细胞发生转化,转化而来的细胞类型很大程度由其所处脑区决定,例如,在纹状体中,iDA神经元即是转化终点。那么这种特异性从何而来呢?
付向东等人发现中脑星形胶质细胞会表达低水平的转录因子Lmx1a和Foxa2;中脑发育过程中,它俩在释放多巴胺的神经元的祖细胞中表达,也是这些祖细胞向神经元发展必不可少的要素。 PTB的离去进一步加强了Lmx1a和Foxa2的表达,像Ctip2和Cux这类与皮质神经元相关的转录因子的表达水平也随着升高。
此外,对黑质或邻近腹侧被盖区(VTA)中的星形胶质细胞进行重编程,产生了iDA神经元的不同亚型:黑质中的Sox6和Aldh1a1,以及VTA中的Otx2。
付向东和同事们的研究结果表明,脑区域特定的转录因子有助于星形胶质细胞向iDA神经元的转化。但杨辉团队的细胞转变是在纹状体里实现的,纹状体的星形胶质细胞不同于黑质及VTA,不会表达Lmx1a和Foxa2这些因子,自然没法用付团队发现的机制来解释。
那么纹状体中导致iDA转换的机制可能是什么呢?
杨辉团队发现接受治疗1个月后的帕金森病小鼠,iDA转换效率差不多提高了2倍。他们提出:在面对内源性的多巴胺神经元缺失时,星形胶质细胞本身或周围环境中的细胞,会表达一些促进星形胶质细胞向iDA神经元转化的因子。换言之,黑质及VTA本身就会表达Lmx1a和Foxa2这些促使iDA转化的因子,在PTB缺失的情况,这种表达还会加强,所以付向东的实验结果水到渠成;而纹状体虽然原本不表达Lmx1a或Foxa2,但在多巴胺神经元缺失的情况下,会启动另一套转录因子分泌程序,这些因子同样可以推进星形胶质细胞向iDA神经元转变,因此杨辉等人也得到了差不多的实验结果。

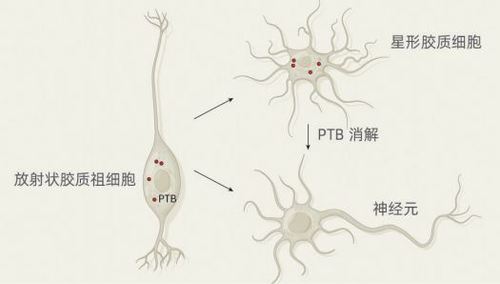
星形胶质细胞向神经元转化的路径。放射状胶质祖细胞是干细胞样细胞,在发育的小鼠中脑里表达着编码PTB蛋白的信使RNA。它们可产生神经元,也可分化出星形胶质细胞这样的非神经元细胞,但星形胶质细胞只有在没了PTB之后才能转化为神经元
分化有先后,PTB有专攻
这些研究引出了一个有趣的问题,那就是为什么星形胶质细胞会不断抑制神经元的基因表达。一种解释指向细胞的发育起源:星形胶质细胞和神经元有共同的祖先——放射状胶质祖细胞,这是一种干细胞样细胞,能够先产生神经元,然后又分化出星形胶质细胞和其他支持神经元的神经胶质细胞。
在处于发育过程的小鼠中脑里,所有放射状胶质细胞类型都可以正常表达Ptbp1基因,而走在分化之路上的神经元前体细胞,和已经分化完成的神经元,则不再表达Ptbp1。其中原因可能在于星形胶质细胞作为放射状神经胶质细胞的后代,已经承继了一套让已有神经元安然休眠的程序——除非PTB消失,休眠才可解除。
另外,Ptbp1基因也会在其他类型的中脑细胞里表达,这些细胞包括血管中的内皮细胞和周细胞,心室腔内的室管膜细胞,以及小胶质细胞(一种免疫细胞)。接下来的研究应重点关注在其他种类的帕金森病动物模型中,PTB的消解是否也能同样带来iDA神经元的转化。
付向东和杨辉等人的策略要在临床上发挥作用,可能需要先提高效率。比方说,注射shRNA的星形胶质细胞最终有60%~65%是不会成为iDA神经元的。若想提高效率,研究者必须让shRNA病毒更集中地靶向黑质里的星形胶质细胞,或再引入某些因子,使得其他非黑质星形胶质细胞也可以转化为iDA神经元。
付向东等人在新发表研究的最后一组实验中,探索了一种实现临床应用的方法:一种称为反义寡核苷酸的短核酸,能与mRNA结合并阻止其翻译出蛋白质。借助该反义寡核苷酸破坏PTB的表达过程或许可以有效实现iDA样神经元的转化。他们最后也确实通过此方法,恢复了帕金森病小鼠的运动行为。
未来的实验将研究人类中脑或纹状体的星形胶质细胞是否也可以转化为iDA神经元,以及转化后的神经元细胞是否可以保持长期稳定,能否精确诱导多巴胺分泌。另外,消解PTB是否有安全隐患,以及怎样制定出一套完善的治疗策略以避免各种健康风险(如星形胶质细胞数量减少的后果),也同样需要研究者花大工夫去琢磨。
总而言之,许多问题等待解决,但此类基因疗法的简便性和高效率,使其极具潜力,有望为治疗像帕金森病这样的神经系统疾病开辟新的篇章。
资料来源 Nature