化学反应时分子究竟是怎样变化的?化学家正在为寻求答案而努力工作。他们设法用量子物理的理论来理解化学反应,至今已有60多年了,现在,现代强大的计算机使理论家能够对最简单的化学反应进行精细的量子计算;同时发展起来的高能激光器使实验工作者能够在实验室里以前所未有的细致程度研究这种反应。一个化学物理学的新时代已显露曙光。
化学家试用各种各样的理论去理解化学反应是如何发生的,其中最为精密的是考虑反应中原子和分子的量子本质。不过,化学反应涉及的不是少数几个原子,其量子理论的复杂程度是吓人的。为了能够应用量子理论,需要先做许多简化和近似的工作。
你可以想象的最简单的化学反应则是一个例外。这里,一个氢原子置换双原子氢分子中的另一个氢原子:
H+H2→H2+H
这种置换叫作氢交换反应。不幸的是,对理论家来说使氢交换反应简化的因素,却是给实验研究者带来极大困难的因素。直到大约6年前,理论家还得不到详细的实验资料来同他们的理论计算相比较,但是现在,应用激光技术上的新突破已经产生出正是理论家所需要的信息,实验工作者业已提供的数据比理论工作者能够推导出来的要多,理论工作者感到压力,非要改进他们的计算不可。这做起来的困难不比做实验少。
在考虑化学反应理论时,化学家们极其重视化学反应中的“跃迁状态”概念。跃迁状态是一种“在中间”(in-between)的结构,它是在原子和(或)分子来到一起形成一种新的排列时出现的,先前化学家认为,由于跃迁状态只不过存在几十毫微微秒(10-15秒),根本无法在实验室里研究它,它不是被隔离开来的单个分子,你无法对它作孤立的研究_然而化学家能够明确指定影响化学反应发生方式的那些性质,在实验室测定这些性质是当今实验化学家面临的最实际的挑战之一。
在氢交换反应中,两种反应的化学形式——氢原子(H)和氢分子(H2)来到一起形成由3个氢原子组成的(H3)跃迁状态,然后重新排列它的键,形成1个新的氢分子和1个氢原子。
H+H—H→H—H—H→H—H+H
相对来说,计算H3跃迁状态是比较容易的,因为它只包含很少几个粒子。1个氢原子由1个质子和1个电子组成。所以H3跃迁状态只包含着3个质子和3个电子。现代量子计算理论恰好能够处理这类很少粒子数的系统。即便如此,还必须做一种道要的近似工作。
一个质子大体比一个电子重2000倍,这就是说在H3系统中质子的运动比电子要慢得很多,我们不妨假设在质子改变它的位置时电子几乎同时要调整位置,以达到用最低的能量来维持其排列。这就是Born - Oppenheimer近似。这使我们能够描绘出一张“轮廓图”或势能面,用以说明H3系统的能量依质子移动而变化的状况,理论,家不必借助于更多的假设和近似就可以相当容易地应用量子理论来计算H3的势能面。在这个意义上氢交换反应是唯一的。
势能面描述了能量同电子和分子相束缚的联系。能量取决于总电子数、电子的空间分布和电子自旋,分子中电子的每一种可能排列都会有一个不同的势能面。但是同样的势能面适用于分子或包含着同位素的反应(同位素是原子核中包含质子数相同但中子数不同的原子),例如,包含1个氢原子和1个氘原子(D)(氘核中有1个额外的中子)的分子,与包含2个普通氢原子的分子一样,具有相同的势能面。
用较重的氘来代替氢使化学家得以弄清反应分子和氢交换反应产物之间的区别。研究所有的反应交换(H+D2,H+HD,D+H2等等),每种反应都给化学家以独立的信息,各个反应都与相同的势能面相联系。
图1表示2个关于H2系统的势能面。在这个系统中氢原子之间有不同角度的键。虽然这些轮廓图主要用于计算机计算,但它们还能帮助我们理解氢原子趋近氢分子时H3系统能量跟着变化的情况。如果氢原子从一旁来与氢分子端头相接,使得3个氢原子成一直线,这时系统的能量增至最大值(见图1a)。黑线表示的是最低能量的路径;任何一个保守的登山者要想通过一个山谷到另一个山谷去,都会寻找一条陡度最小的路径。最小能量路径中的最大点称为“鞍”点。鞍点处H3系统的性质说明了反应的跃迁状态,越过鞍点之后,H3系统“滑下山”来,得到了反应的产物。
你可以把这个反应过程设想成一条由大理石在一平面上滚动时所画出的路径。大理石画出的“轨道”可以应用牛顿运动定律从初始位置和初始速度中计算出来。与此类似,化学家可以算出势能面上化学反应的轨道。把范围广阔的各种起始条件的大量轨道加以平均,就能够得到充分的信息,足以预示反应中发生的情况。
不难看到,这种处理方法的基础是经典物理。但是,原子和分子当然服从量子力学定律。这就是说它们的能量不是连续变化的;它们只有一些特定的值,这些值是按梯级或按量子数一步步升高的。这不仅适用于一个原子或分子中电子的能量,也适用于它们所能碰到的所有运动形式:平移、振动和转动,我们注意一个H3面的二维片(见图1e),1个氢原子离2个束缚着的氢原子很远,这里可以看到上面所说的效应,这个曲线实际上说明:势能怎样随氢分子中两个原子间的距离而变化。当原子靠近到足以形成键时能量落到了最低点,但是距离更加靠近时,由于带正电荷的原子核间的斥力,能量又升高了。在较大距离处,能级截止,这与化学键断裂相当。
化学键的作用很像一个小弹簧把原子核互相拉在一起,以使分子振动,量子力学预示,振动产生一组在势能曲线内的分立能级(见图1e)。每一级相当于一次不同量的振动激发,激发中原子核在它们的最低能量位置附近来回运动。每一级联系着一个数字,叫做振动量子数γ。每一振动级有一组紧密而分离的能量级,这是由氢分子在空间的转动所产生的,每一转动级有一转动量子数j。分子的平移运动也分成级,但是它们靠得很紧,其效应同连续的一样,所以可以忽略不计。这样我们就可以用一组特定的关于电的、振动的和转动的量子数来描写氢分子的总能量。这些量子数就确定了分子的“量子状态”。
在计算氢交换反应的轨道时,理论家考虑粒子的量子本质,办法是只选择与反应氢分子的量子状态能量相匹配的那些始发条件。接着按照牛顿定律计算轨道,测定生成氢分子的能量,再赋予它最接近的量子状态。由于这种计算把经典描述和量子描述结合起来,所以称之为准经典轨道计算。
化学家非常感兴趣的是从一特定的反应分子的量子状态到一特定产物的量子状态的反应快慢——“状态到状态”的反应逨率。他们还对在终了产物状态中所形成的分子数(产物状态分布)感兴趣。多年来,理论家已能计算氢交换反应的状态到状态速率和产物状态分布。可是直到最近,他们还没有得到相应的实验数据来核对他们的理论计算的精确程度。
原因在于氢交换反应似乎太简单了。要测量状态到状态速率和产物状态分布,实验工作者须能监控由氢交换反应形成的个别氢分子的量子状态,在别的反应中,实验工作常常可以做到这一点,办法是对生成分子的各种波长的吸收光和发射光进行研究,如果吸收的或发射的光能量同分子中电子之间的能级差相匹配,那么实验工作者就能在紫外光和可见光的范围内测量电子的吸收和发射光谱。振动和转动的能级之间的差所产生的吸收光谱则是在红外和微波的范围。这些光谱能够提供生成分子可能能量的大体上完整的图画。
然而就氢分子来说,有一个障碍。因为要分子吸收辐射,就要让它“激发”到更高的振动能级或转动能级,这需要一个不均匀的电子分布——一个电偶极子,它能同电磁辐射的电分量相互作用,而氢分子是对称的,它的电子相等地分配在原子核之间,因此没有永久的电偶极子,也就不会有振动或转动的吸收光谱。
解决这个问题的一种方法是应用能量高得多的光,这个光激发分子中的一个电子到更高的电子状态,这样你就可以得到关于振动和转动状态的信息,办法是测量有多少光被吸收,或者当电子接着落回到较低电子状态的不同振动能级和转动能级时测量分子的发射,不过这类研究所需要的光波长是在远紫外区,常规的光源对这一范围是不适用的。
1983年,加里福尼亚两个实验室的研究人员用高能激光产生紫外光脉冲来解决这个难题,在伊尔文的加里福尼亚大学的詹姆斯 · 法仑德尼和丹 · 日里德应用一种叫做反斯托克斯 - 拉曼的光谱技术去测量由反应氢原子和氘分子产生的氢 - 氘分子中的量子状态分布。倪仲庆、D. 费里普斯和H. 拉文也同法仑德尼一起工作,应用和发展了这些技术,斯坦福大学的R. 赛和他的同事E · 马仑奈罗和C. 雷脱诺改进了一种叫做多光子电离的技术,它用紫外光来检测各量子状态中的终了氢氘分子,从那以后,R. 布雷克,K. D. 林耐和D. 克林诺就同赛一起共同进行氢交换反应的研究。
两组研究人员首先应用激光击破含氢分子(如氢的碘化物)产生出氢原子。由于它们供给的能量比击破分子所需要的多,结果氢原子带着过剩的能量使自己的运动变得很快,快速运动的氢原子把自己的能量增加到反应氢分子上去,给H3系统提供了总“碰撞”能量。你可以选择不同的含氢分子或选择击破它们的不同的激光波长来改变和调整碰撞能量。
这两个组一直在精化和发展他们的技术。最近,他们已得到互相吻合得极好的结果。这两种实验技术的处理过程和获得信息的方法是十分不同的,他们能分别得到这样吻合的结果,实在令人高兴。
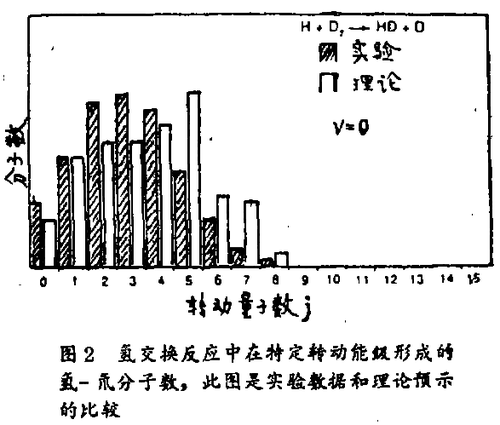
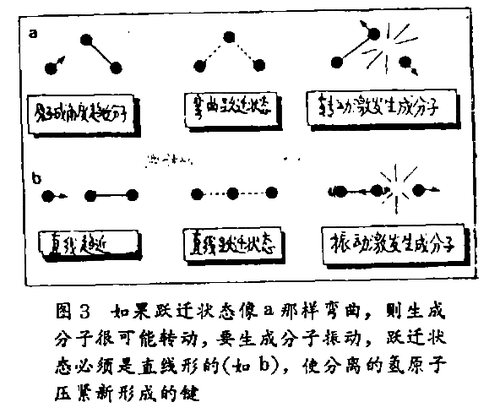
图2是赛组在斯坦福所得到的这类数据的一个例子。法仑德尼组获得更详细的数据,两者的结果是相等的。这个图表示在特定的转动(j)和振动(v)能级下形成的氢 - 氘分子数对于j(对每个v)的关系。这些结果说明分子形成时通常设有激发到更高的振动能级,在每一振动能级中转动激发也是很微弱的。这是因为H3势能面的形状表示鞍点的能量,说明反应的跃迁状态H—H—H为直线排列时是最低能量,在跃迁状态中对这种形状的偏爱意味着要把能量转换成终了分子的转动是困难的。要使生成分子转动,一个容易得多的办法是让分离出去的氢原子以一个斜角“踢”它一脚(给一反冲)。见图3a。
振动激发的缺少表示H3系统在反应分子演变为生成分子时并不偏爱于开启振动量子状态。当振动激发从v=0增加到1,又增加到2时,振动激发数减少。这又一次说明跃迁状态的原子偏爱于在一条直线上。要在产物中获得任何振动激发,H3系统必须是直线型的,以使分离的氢原子冲击中心氢原子,压紧新形成的氢 - 氢键。见图3b。
最近,斯坦福有更多的实验说明氘原子和振动激发的氢分子之间的反应比它和未激发的氢分子的反应在形成的氢 - 氘分子中给出更高的转动激发,研究者们对这一现象的解释是,振动激发的氢分子中的氢 - 氢键平均来说比未激发分子中的键要长,所以当原子在跃迁状态时保持一个角度时,反应进行得十分令人满意。
用紫外激光从氢分子中产生的初始原子可以成为很快速的运动原子,这就是说在交换反应中它们同分子发生高能碰撞。要对在如此高碰撞能量的氢交换反应下发生的事情作出可靠的计算是困难的。但是理论家应用量子力学很快找到了计算的手段。不过准经典轨道计算相对来说要简便一些。图2表示N. 布拉易斯在阿拉莫斯国家实验室和D. 托赖拉在明尼苏达大学的计算结果。考虑到这些计算背后的近似和假设,实验结果和理论结果之间的吻合是显而易见的。
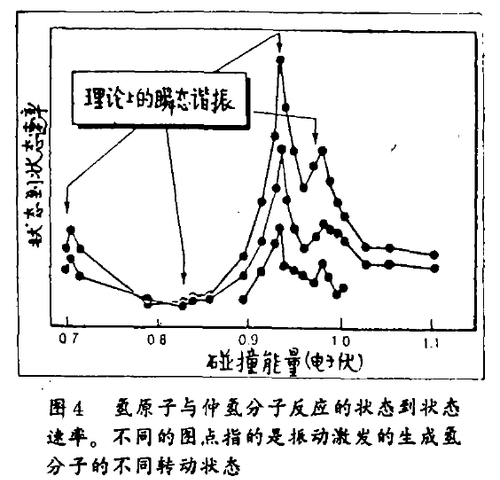
就在最近,倪和法仑德尼获得了他们认为是H3跃迁状态的证据。他们研究了氢原子和仲氢分子(在这里2个质子反向自旋)之间的反应,测量了许多不同碰撞能量下振动激发形成时的状态到状态速率,如图4所示,一些能量比另一些能量给出更高的速库。开初,倪和法仑德尼认为这些是“瞬态谐振”(dynamic resonances)——当振动激发跃迁状态形成时产生速率增强。虽然跃迁状态只保持几十个毫微微秒,但已足够它在结束之前振动三、四次了。理论家们预言这样的谐振至今已有20多年了。
然而赛和他的研究组对倪和法仑德尼对结果的解释提出强烈的异议。现在法仑德尼认为,虽然他的结果提供跃迁状态的证据,但它们所反映的可能比瞬态谐振的直接影响有更为精妙的东西。这就有待进一步的研究了。
实验工作在6年中已走过很长的路。高能激光器已经打开氢交换反应的心脏。尽管准经典轨道计算与实验结果符合得很好,理论家们仍须发展他们的技术以对高碰撞能量进行状态到状态的完全的量子计算。
实验化学家也需要做更多的工作。他们正在进行的对H3跃迁状态性质的实际测量有待完成。更多的证据积累意味着化学家们对它作了60多年的设想最终将要变成现实。深入的研究正在赛和法仑德尼两个实验室里进行,最简单的化学反应中还蕴藏着化学家们渴求发现的更多的秘密。
[New Scientist,1990年5月12日]