含锡和汞等元素的催化剂能加速化学反应,但也污染了环境。化学家们发现,酶是其最佳的替代物。
本世纪,为满足人类对更好的食物供给,更有效地防御疾病,更舒适的生活,化学家们认为他们比任何人都做了更多的工作。但是,我们也知道由此造成的环境污染是非常严重的。现在化学家们正在寻找无污染的新分子,用以改善我们的生活,一些人认为酶可能是合适的选择。
化学家们合成的有用分子大部分是有机分子,比如药物和农药,主要是由碳和氢原子组成。化学家们由简单易得的原料开始,经一系列步骤合成它们。但是离开了催化剂的帮助,这些步骤中的一步或多步将变得非常缓慢,常常慢得使该反应没有什么意义。过去,化学家们用含有诸如锡和汞的重金属化合物作为催化剂。现在,他们注意到这些金属有时会对土壤、河流和海洋产生很大的破坏作用,他们正在寻找无污染作用的催化剂来替代这些重金属化合物。
这种催化剂正是酶。它是天然的催化剂:植物、动物和微生物都依赖于它。实际上,所有的微生物化学反应也都依赖于酶。它加速分子的分裂或结合过程,催化调节能量消耗和积累的循环过程。离开了酶,生命将不会存在。地球上有7000种左右的酶,生物化学家已确认了其中的2/3。酶催化许多有机分子参与的多种变化,因而,化学家们对研究酶在非生物反应中的应用非常感兴趣。
由酶的名称便可知道它的功能,大部分酶的名称是根据它所作用的分子确定的,后缀“酶”表示它催化这种分子的裂解。例如:蛋白酶催化蛋白质的水解;脱氢酶使氢离去;酯酶催化酯水解为它的组成部分羧酸和醇。然而,在某些条件下,酶也能催化反方向的反应,生物学家们已经发现:DNA聚合酶催化较小的脱氧核糖核酸单元(DNA)和带有遗传密码的分子结合。分子生物学家们用DNA聚合酶成千上万次地复制DNA碎片。
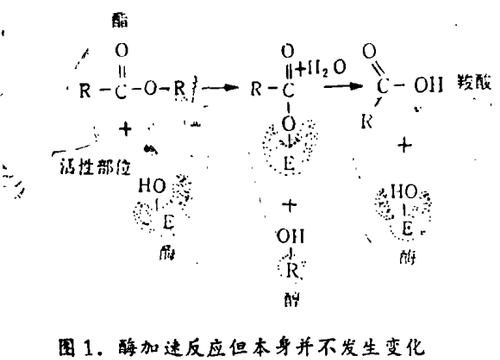
酶是真正的催化剂,它通过降低反应的能量而加速反应,但反应完后本身并未发生改变。它们有如此明显的催化效果与其分子结构有密切的联系。所有的酶都是很大的蛋白质分子,它们由链状排列的氨基酸分子以复杂的方式折叠形成。酶最重要的部分是其表面称为活性部位的特殊部位,当酶与一形状适合其活性部位的分子相遇时,酶能以最适合该分子发生反应的方式与其嵌合。一些研究者们认为:酶在与特定的分子(它所作用的底物)结合时,会使底物形状发生微妙的变化。许多酶在活性部位有易变形的环状结构,这一结构的变化取决于底物的形状。另一些研究者认为:底物正好嵌入酶的活性部位,好像钥匙插入锁内。
最后的结果是一致的:当底物反应完后,它就具有不同的形状了,这时它就不再适合于酶的活性部位,酶释放它得到产物(见图1)。在本世纪60年代,包括诺贝尔奖获得者V. 普雷克(V. Prelog)在内的许多化学家们开始认识到:这样的反应历程可能是非常有用的。一种酶只能与一种特定的分子结合,这种分子适合于酶的活性部位。化学家们可利用酶作为精确的工具来合成其它分子。随着研究工作的深入,化学家们发现:酶的性质使其具有超过人工催化剂的独特优势。
大多数酶在非常温和的条件下起催化作用——约35°C、常压和中性介质。酶催化反应不仅不需要复杂的仪器装置,而且非常节约能量。例如:为合成对许多反应都是非常有用的起始原料甲醇,化学家们让甲烷和氧反应。为此需进行两步反应。第二步要在450—500°C,300 atm和铬/锌氧化物催化剂存在下进行。即使这样,在第一步反应完后,第二步也只能将约15%的第一步产物转化为甲醇。在自然界就不存在这样的问题,一种称为单加氧梅的酶可使这一反应很容易地进行。难怪化学家们在寻找用酶作为工业过程催化剂的方法。
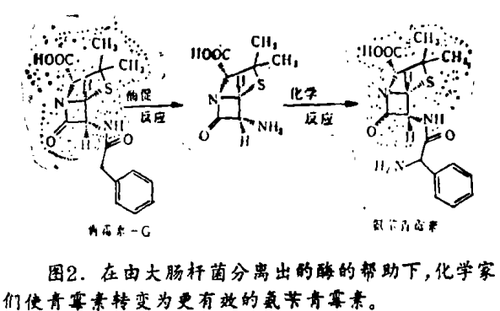
酶在温和的条件下起作用,因而,有时它是必不可少的,正像研究者们在研究青霉素 - G时所证实的。青霉素 - G含有称为β - 内酰胺的四员“环”,还有其它原子(包括氮、硫和氧)与环相连(图2),因而它能杀死细菌。β - 内酰胺环妨碍了细菌细胞壁的生成,致使细菌极易被杀死,早在本世纪50年代,布里特斯(British)公司比彻姆(Beechams)药物商行的科学家们已注意到:只要能用更复杂的基团取代β - 内酰胺环上的一个基团,他们便能合成更有效的抗生素。问题是如何在不破坏敏感的β - 内酰胺环的前提下做这一修饰。由微生物大肠杆菌中分离出的一种酶使这一问题得以解决。它们催化不需要基团的离去,科学家们在这一部位“缝合”新的基团,形成抗细菌化合物氨苄青霉素,胸腔或膀胱感染的病人对这种药是很熟悉的,J · 鲍德温(J. Baldwin)和牛津大学的小组对有关研究有新的进展,现在鲍德温的小组利用酶从简单的三肽(由三个氨基酸线性相连而成三肽)便能合成天然的新青霉素。这些巨 - 青霉素将有助于控制诸如败血病等其它药物无效的细菌感染。
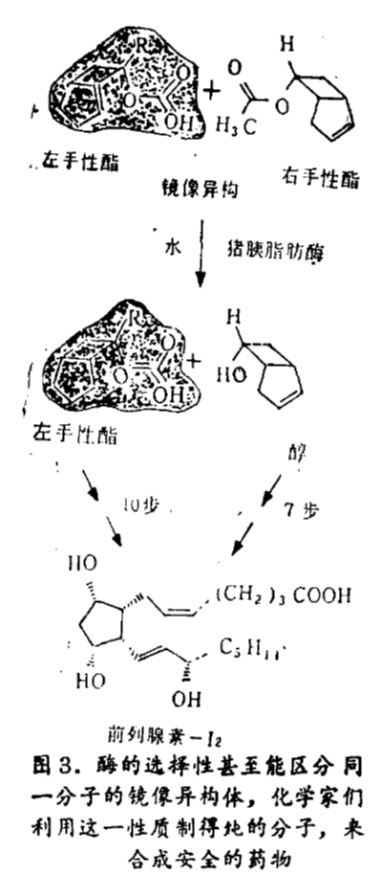
对于精细(高纯度)化工和药物工业,酶具有使它们满意的最大优点——立体选择性。这是使“左手性”和“右手性”混合物分离的一种能力。它是人造激素合成方法的基础。在人体内的许多反应中,称为前列腺素的一类激素起分子“传输控制”的作用。其中一种是前列腺素 - I2,人体缺乏它就会得心脏病。但由于它不稳定,在起作用前便分解,医生不能开这样的激素药方。将来,医生便可使用人造敝素,它不仅稳定,且在体内与天然激素一样起作用。为了安全起见,这种人造激素必须模拟天然激素到很高的程度,即不能被它的镜像异构分子所污染。
为使人造前列腺素 - I2达到这样的纯度,化学家们从给出等量酯(由酸和醇形成的有机盐)与其镜像体的反应开始。由猪的胰腺提取到猪胰脂肪酶。他们利用了这种酶和水。酶催化“右手性”酯分子转变为醇,使“左手性”酯分子和“右手性”酯分子分离,这是化学药品办不到的。酶的专一性确保了剩余的酯分子都是“左手性”的。在随后的一系列步骤中,化学家们使这些纯的产物,酯或醇,转变成人造前列腺素(图3)。
为普及与上述使用酶提纯左手性醏相类似的方法,而制取纯手性化合物,麻省理工学院的A. 克利巴诺夫(A. Klibanov)及其同事们做了许多工作。如上所述,这样做是完全可能的。酶促使反应进行的方向与它们在催化自然界化学反应时的作用有关。酶已进化了相当长的时间,以至人们发现自然界以最经济的方式使用它们后并不感到意外。令人惊奇的是:酶与人造分子(一些只能在化学实验室见到的酯)作用时的方式和与天然分子作用时的方式是一样的。
在本世纪初,科学家们已经认识到:胰脂肪酶不仅能催化酯水解成醇,而且可催化它的逆反应:在少许水存在下,醇和羧酸结合形成酯。1984年,在微量水存在下,并添加酵母脂酶,克利巴诺夫用左手和右手性羧酸混合物与醇反应。酶催化右手性的酸分子和醇结合形成酯,但左手性羧酸并未发生反应,化学家们能使脂和纯的左手性酸转变为更吸引人的化合物。
食品化学家们经常用酶催化一系列反应中的关键步骤。某反应的关键步骤是由一组称为肽酶的酶催化的肽键形成过程。肽键是使氨基酸单元连接起来形成二肽、寡肽、最终形成蛋白质的碳 - 氮 - 碳键。二肽天冬酰苯丙氨酸甲酯(Aspartame)由于有甜味,被食品化学家们广泛地使用,并以Nutrasweet被大多数人熟知。它是在肽酶嗜热菌蛋白酶的帮助下合成的。实际上,它在无意中成了走俏的商品,有人偶然发现它很甜,虽然英国的ICI公司首先生产了这种二肽,但它最吸引人的性质是由美国药物公司化学家瑟尔(Searle)发现的。他在拿起滤纸前有舔手指的坏习惯。一天、他舔食了微量的天冬酰苯丙氨酸甲酯,这是偶然发现珍宝的运气,但并不能推荐为试验新药品的最佳方法。
所有这些酶催化反应或生物转化过程是极易做到的,不需要任何特殊的仪器,只要买几瓶纯净的酶即可。由于一些反应依赖于有添加剂的酶,它们变得非常复杂,这些外加的成分参与催化过程。这些外加成分可以是金属原子如铁、称为辅助因子的非蛋白质小分子,或二者均有,许多维生素和其它物质是我们食物中的微量成分,它们实际上就是辅助因子。事实上,辅助因子做了许多工作。催化过氧化氢分解的酶就要铁原子作为辅助因子,它们所含的简单铁化合物具有相似的效应。
对于这些较复杂的反应,化学家们喜欢用有现成的酶及辅助因子的全微生物。微生物Thermoanaerobium brockii含有一种醇脱氢酶,由该名称可知它催化醇除去氢的反应。在适当的条件下,这种酶也可催化相反的反应:酮(含有碳氧双键的分子)加氢生成醇。进行这一反应需要一种称为二氢烟酰胺腺嘌呤二核苷酸磷酸或NADPH的分子。NADPH是一种最常见的辅助因子。它的主要功能是传递氢原子,在传递过程中它转变为烟酰胺腺嘌呤二核苷酸磷酸(NADP)。
面包酵母和其它微生物对于涉及加氢的反应是特别有用的催化剂。酵母细胞含有合适的酶和烟酰胺腺嘌呤二核苷酸类的一种辅助因子。有机化学家们用酵母来大量制取纯的3-羟基丁酸酯,它是一系列类似分子的一种,由于它们的不对称性或手性,被广泛地用作构造材料。
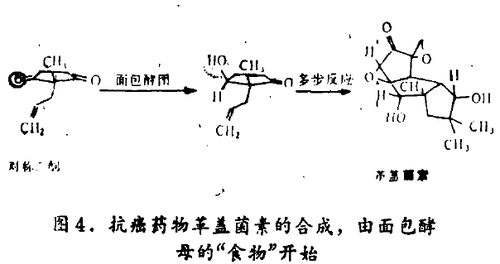
在化学家们合成天然分子的过程中,手性化合物是重要的起始原料。这样的分子常常是极其复杂的,它们在生物系统内以独特的方式起作用。用以治疗癌症的革盖菌素就是一例。它由三个稠合的碳原子环组成,在80年代中期,芝加哥阿博特实验室的D. 布鲁克斯(D. Brooks)由含有两个酮基(氧原子通过双键与碳原子相连)的五碳环分子出发经一系列步骤合成了革盖菌素,两个酮基在五员环的两侧呈对称结构。简单的面包酵母提供了合适的酶,催化其中一个酮基加氢形成羟基(图4)。
化学家们的手头有数千种物质可以完成这一转变,但没有一种只选择五员环上的一个氧原子进行反应。在得到只含有一个双键氧原子的五员环后,化学家们便能合成革盖菌素。化学家们又一次利用酶在特定的原子上进行有目的的反应,得到预期的产物。
有关类固醇化合物的研究很大程度上得益于酶的帮助。类固醇是以一四环稠合碳架为基础的复杂有机大分子。它们包括许多激素、维生素D以及消化体内脂肪的胆汁酸。密执安州,卡拉马祖(Kalamazoo)、厄普约翰(Upjohn)实验室的研究人员,在微生物Rhizopus arrhizus的帮助下,将类固醇孕酮转变为消除炎症的有效药物。由于这一转变涉及添加氧原子到几个可能部位中的一个部位,离开酶的帮助便不可能实现。化学试剂添加氧原子时没有这种辨别能力。但在化学家们能应用这一技术制取其它精细化学品之前,他们还需做更多的研究。因为在比类固醇复杂的分子中,即使酶也会添加氧原子到多于一个的部位。
伦敦帝国学院的S. 利(S. Ley)及其同事们,帝国化学公司(ICI)特斯德(Teesside)实验室的S. 泰勒(S. Taylor)等人进行研究时,他们利用微生物及其酶优于化学品的特性,来复制在中枢神经系统起化学信使作用的分子。首先,ICI的小组通过滴加假设的起始物(苯),从土壤中分离出了“菌”。以苯作为能量来源的微生物迅速繁殖,科学家们收集起来后在实验室培养它们。接着用苯喂养这些“驯服了的”菌,便可得到产物。与菌有关的酶添加两个羟基到苯上,形成环己 - 3,5 - 二烯 - 1,2 - 醇。现在,利的小组有充裕便利的起始原料来源,可用以制取信使分子。
美国哈佛大学的G. 怀特赛德(G. Whitesides)利用兔子肌肉的醛缩酶来催化新碳 - 碳键的形成。由于这种酶促使葡萄糖的分解,它催化提供肌肉运动能量的反应。由于醛缩酶催化的反应在两个碳原子间成键时,它们可以成为手性中心,也就是说,该反应给分子以“手性”,所以怀特赛德对醛缩酶特别感兴趣。这样的反应是有机化学的中心。
实业家们已利用类似的反应作为生产天然物质的较好方法。例如:利用称为异构酶的一种酶来使果糖转变为更有用的葡萄糖。利用更复杂的技术,应该能以类似的方式制造出精细化学品,而对环境没有污染。生物技术专家和化学家们在制取所需要的酶方面已做得很出色。最近的研究主要集中在以下四方面:一些科学家正在寻找新的微生物;一些科学家在研究利用现有的酶来制取药物和农业化学工业上有用的分子;另一些研究在特殊环境下酶的行为,例如它们在溶剂体系而不是水中使用时的情况;还有一些有趣的研究是多种酶的“一锅”混合,它们一起参与作用形成联串反应——一反应的产物是下一反应的起始物。每一类型的酶催化联串反应中的特定步骤,互相并不干扰。如果所有这些研究得以实现,酶便能铺设通往化学新境界的道路,从而使人类的生活水平不断提高。
[New Scientist,1990年4月21日]